Dua Kandidat Vaksin Covid-19
Pengembangan vaksin terus dilakukan untuk menghadapi pandemi Covid-19. Hingga 4 April 2020, WHO mencatat ada 62 kandidat vaksin yang diteliti, dua diantaranya telah menjalani uji klinis.
Direktur Deteksi Antibodi dan Pengembangan Vaksin Nita Patel mengamati model komputer yang memperlihatkan struktur protein dari vaksin potensial untuk Covid-19 di laboratorium Novavax di Rockville, Maryland, Amerika Serikat, Jumat (20/3/2020).
Sebagai respons kasus pneumonia yang penyebabnya belum terdeteksi pada 31 Desember 2019, Organisasi Kesehatan Dunia (WHO) memberikan respons cepat dengan mengaktifkan cetak biru penelitian untuk mempercepat penemuan vaksin virus korona baru.
Dalam pengembangannya, WHO mencatat, hingga 4 April 2020 sudah ada 62 kandidat vaksin Covid-19 yang diteliti. Dua di antaranya telah menjalani uji klinis.
Dokumen cetak biru diaktifkan khusus untuk penyakit atau patogen prioritas dalam konteks darurat kesehatan masyarakat. Total ada delapan penyakit yang menjadi prioritas penanganan oleh WHO, salah satunya adalah Disease X.
Jenis Disease X merujuk pada epidemi atau pandemi serius yang dapat muncul disebabkan patogen yang saat ini belum diketahui dan mampu menyebabkan penyakit pada manusia. WHO menilai, pandemi wabah Covid-19 menjadi fokus utama saat ini sehingga cetak biru penelitian diaktifkan.
Sebagai upaya percepatan penanggulangan suatu wabah, cetak biru memiliki jadwal ketat berbasis tema penelitian. Khusus Covid-19, alur penelitian komprehensif mulai dari vaksin hingga pengobatan dilakukan dalam durasi satu tahun, yaitu mulai Februari 2020 hingga Februari 2021.

Para ilmuwan bekerja di laboratorium Vaksin dan Penyakit Menular-Pusat Vaksin Internasional atau VIDO-InterVac. Foto diambil pada 18 Oktober 2019. Saat ini laboratorium yang berada di Universitas Saskatchewan, Kanada, itu tengah meneliti vaksin untuk Covid-19.
Februari 2020, agenda global fokus pada tahapan Global TPP (target product profile) building on experience from MERS and Disease X. Seluruh instansi penelitian medis berusaha untuk mengenali dan membangun protokol penelitian Covid-19 berbasis kasus MERS dan penyakit-penyakit baru.
Tahap berikut, Maret 2020, kriteria vaksin makin diperjelas melalui evaluasi mendalam, termasuk desain dan platform yang akan dibangun. Proses tersebut dijalankan dengan melakukan model pendekatan lanskap karakteristik hewan.
April 2020, riset vaksin sampai pada tahapan Assay development and validation required for vaccine R&D dan Vaccine Phase 2b/3 Master Protocol. Tahapan medis pengembangan Assay merujuk pada prosedur dalam biologi molekuler untuk menguji dan mengukur aktivitas bahan biokimiawi di dalam suatu organisme.
Pengembangan Assay dilakukan seiring perumusan kriteria untuk validasi vaksin. Setidaknya ada dua validasi utama, yaitu aman dan efektif serta manfaat lebih tinggi dari risiko. Agenda lain yang dikerjakan adalah memetakan sejarah alami virus korona. Kajian tersebut akan mengungkap bagaimana transmisi virus dan diagnostiknya.
Sejarah alami virus, transmisi, dan diagnostik dilakukan secara mendalam hingga Juli 2020. Setelah dokumen selesai, penelitian akan berpindah pada perumusan kode etik dan pengujian pengobatan yang efektif hingga Februari 2021.
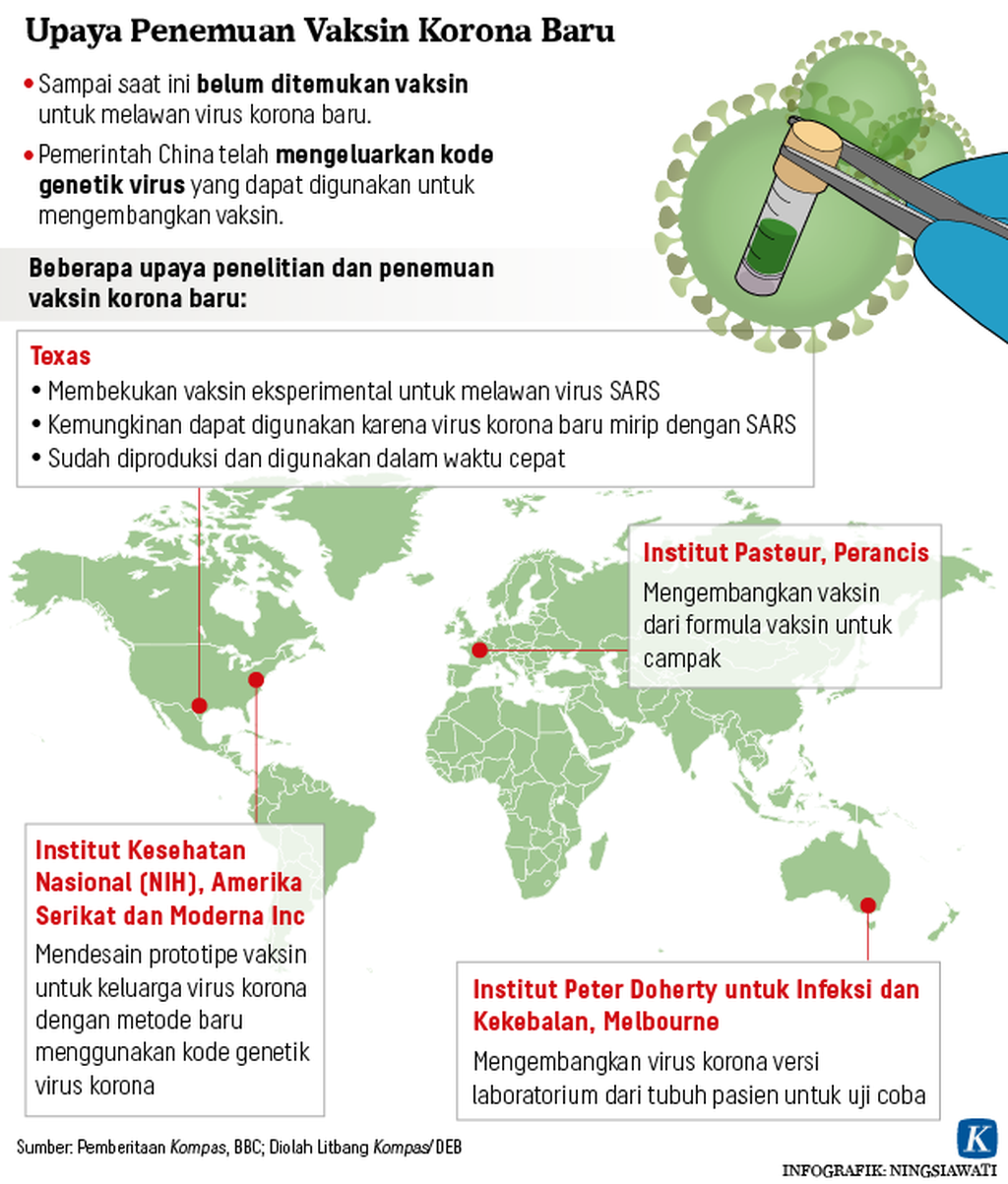
Kandidat vaksin
Percepatan penelitian dan pengembangan penyakit korona Covid-19 melibatkan puluhan lembaga dan universitas di seluruh dunia, di antaranya Global Research Collaboration for Infectious Disease Preparedness, Centers for Disease Control and Prevention, Imperial College London, Johns Hopkins School of Medicine, University of Oxford, dan Unicef.
WHO mencatat semua kandidat vaksin dari seluruh dunia. Dari semua kandidat, dua jenis vaksin sudah memasuki tahapan fase 1 uji klinis, sementara lainnya masih pada fase praklinis.
Kandidat vaksin pertama yang sudah masuk fase 1 uji klinis dikembangkan oleh Institut Alergi dan Penyakit Infeksi Nasional Amerika Serikat (NIAID) bekerja sama dengan perusahaan bioteknologi Moderna Inc di Amerika Serikat. Vaksin tersebut terbuat dari susunan genetik berupa RNA yang bertipe LNP-encapsulated mRNA dan diberi nama mRNA-1273.
Kemampuan RNA dijelaskan mampu menghentikan gerak gen patologis dan mendukung tahapan pengobatan yang diberikan melalui adaptasi gen dan antibodi. Penggunaan vaksin secara klinis perlu didukung dengan sistem pengiriman gen nonvirus yang tepat. Sistem nanopartikel lipid (LNP) saat ini adalah sistem pengiriman utama yang memungkinkan pengobatan berjalan efektif, termasuk eliminasi gen patologis.

Seorang ilmuwan bekerja di laboratorium MIGAL Research Institute di Kiryat Shmona di Israel, Minggu (1/3/2020). MIGAL menjadi salah satu lembaga yang sedang mengembangkan vaksin untuk Covid-19.
Dalam perkembangannya, NIAID mengumumkan telah melaksanakan uji terhadap manusia pada 16 Maret 2020. Uji klinis dilakukan kepada 45 orang berusia 18-55 tahun dan dalam kondisi sehat.
Evaluasi pemberian dosis dilakukan selama enam minggu. Evaluasi uji terhadap manusia dilakukan dalam beberapa skenario dosis yang berbeda-beda. Hal tersebut bertujuan untuk mendapatkan data tingkat keamanan dan kemampuan vaksin guna mendorong respons sistem imun manusia.
Vaksin kedua dikembangkan oleh CanSino Biological Inc dan Beijing Institute of Biotechnology di China yang menggunakan bahan non-replicating viral vector dengan tipe vaksin Adenovirus Type 5 Vector.
Adenovirus Type 5 Vector memiliki salinan biokimia yang serupa dengan pengobatan ebola. Tipe adenovirus adalah salah satu vektor yang paling banyak dieksploitasi untuk pengembangan virus, salah satunya virus HIV.
Kelebihannya terletak pada kemampuan untuk berkembang dengan cepat dan stabil dalam tubuh manusia serta memiliki pola antigen yang spesifik bagi virus. Dalam fase terapi gen untuk pengobatan atau imunisasi, adenovirus bersifat aman.
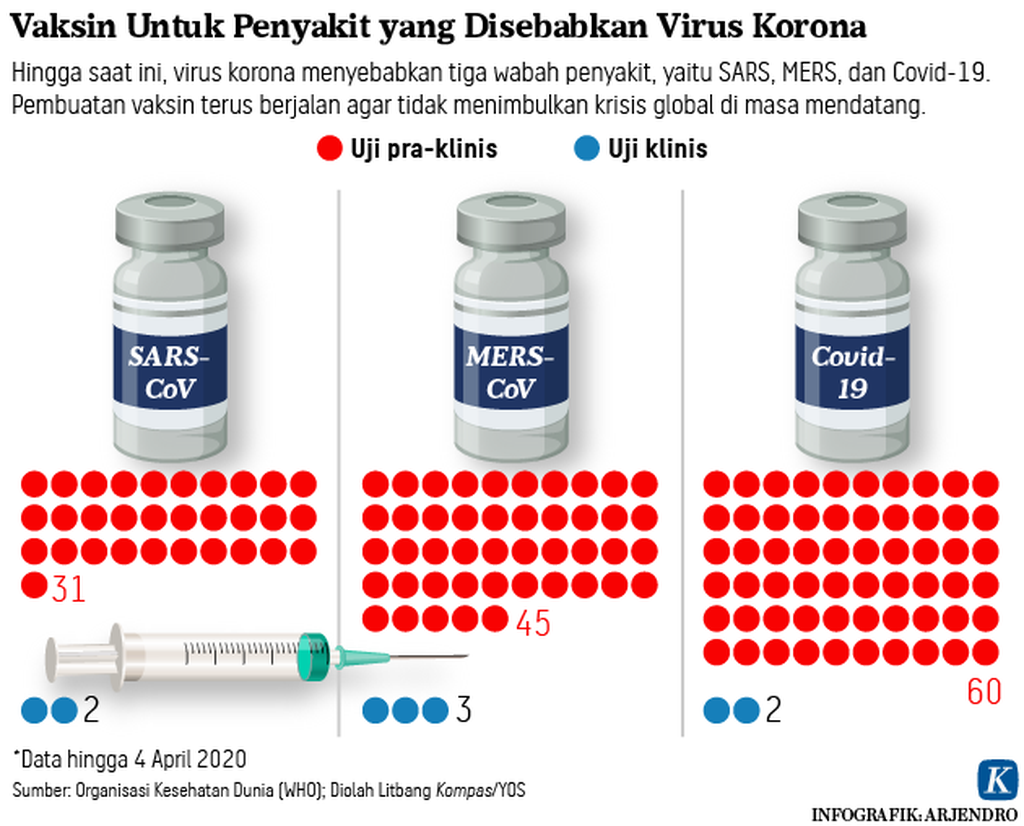
Pengembangan vaksin
Semua kandidat vaksin dikembangkan melalui berbagai macam platform, mulai dari berbasiskan DNA hingga materi yang belum teridentifikasi. Platform penyusunan vaksin virus korona paling banyak menggunakan protein subunit (36,51 persen).
Pengembangan vaksin tidak dapat dilepaskan dari informasi genetik patogen yang sedang mewabah. Vaksin subunit berbasis protein berisikan protein spesifik yang diisolasi dari patogen dan tidak mengandung partikel dari virus.
Dari semua kandidat, dua jenis vaksin sudah memasuki tahapan fase 1 uji klinis, sementara lainnya masih pada fase praklinis.
Selain platform protein subunit, vaksin juga dibuat dari materi RNA (14,29 persen), non-replicating viral vector (12,70 persen), dan DNA (7,94 persen). Persentase pembuatan vaksin yang terbuat dari materi yang belum teridentifikasi 9,52 persen atau 6 kandidat.
Sebelum vaksin diberikan secara massal, uji laboratorium secara intensif harus dilakukan meski membutuhkan waktu beberapa tahun. Saat uji klinis terhadap manusia dilaksanakan, maka tahapan evaluasi dan pengawasan harus dilakukan secara berkala dalam waktu tak singkat.
Lisensi vaksin tidak mudah didapatkan. Efektivitas dan keamanan produk sangat menentukan keberlangsungan hidup manusia. Pada beberapa kasus, ahli virologi meyakini bahwa penelitian tentang vaksin dapat berjalan satu dekade.

Seorang karyawan perusahaan biofarmasi Jerman, CureVac, menunjukkan alur kerja penelitian pada vaksin untuk penyakit Covid-19 di sebuah laboratorium di Tuebingen, Jerman, 12 Maret 2020.
Meskipun ampuh untuk mencegah penularan wabah, penemuan vaksin membutuhkan waktu selama berbulan-bulan, bahkan bertahun-tahun. Ilmuwan harus menyelidiki wabah penyakit dari awal. Selain itu, vaksin juga harus diuji secara ekstensif pada hewan dan manusia. Untuk tahapan ini, minimal dibutuhkan waktu satu tahun hingga vaksin dapat diedarkan di masyarakat.
Pada kejadian wabah SARS tahun 2003 dibutuhkan waktu 20 bulan dari rilis kode genom virus untuk menghasilkan vaksin yang siap diujicobakan kepada manusia. Pada epidemi virus zika, peneliti membutuhkan waktu enam bulan untuk mengeluarkan vaksin.
Vaksin yang ditemukan pertama kali oleh Edward Jenner pada 1796 telah berhasil mencegah berbagai penyakit, seperti tetanus, hepatitis, polio, serta wabah ebola dan flu burung. Vaksin-vaksin tertentu wajib disuntikkan ke tubuh pada saat anak berusia balita.
Baca juga: Memahami Karakter Virus Korona
Penemuan vaksin menjadi bagian dari linimasa munculnya penyakit di dunia. Hingga saat ini, WHO mencatat 26 jenis vaksin telah berhasil dibuat berdasarkan jenis penyakit, seperti kolera, hepatitis, influenza, malaria, dan demam kuning.
Saat terjadinya wabah penyakit menular, seperti virus SARS-CoV-2 penyebab Covid-19, upaya penemuan vaksin menjadi harapan pencegahan penyebaran. Sebab, vaksin dapat memberikan sistem kekebalan dalam mengenali dan membangun pertahanan melawan bakteri atau virus penyebab penyakit. (LITBANG KOMPAS)
Baca juga: Mengapa Harus Membayar Berita Daring?